化学 塩素の製法
までの、の実験において、とともによく使用される薬品である。 初めの洗気びんには〔 水 〕が入っていて, Cl 2に混ざってくる水に溶解しやすい 〔 塩化水素 HCl 〕ガスを吸収させる。 つまり、単数と同じ扱いになるのです。
7
までの、の実験において、とともによく使用される薬品である。 初めの洗気びんには〔 水 〕が入っていて, Cl 2に混ざってくる水に溶解しやすい 〔 塩化水素 HCl 〕ガスを吸収させる。 つまり、単数と同じ扱いになるのです。
7
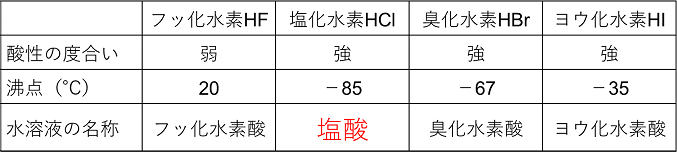
塩酸や硝酸は、気体を水溶液にしたものなので 気体が抜けて薄くなってしまいます。 そうなると布が焦げ始めて穴が開きます。 その他,フッ化水素は他のハロゲン化水素と次のような性質に違いが見られる。
20塩素の捕集法で一番適するものは何か。 そのため、天然では、ハロゲンは鉱物(ホタル石 CaF 2 、岩塩 NaCl)として存在している場合も多い。 反応性が高く、いずれの単体も有毒である。
5その他 塩素はさまざまな金属と反応して塩化物となる。 もっとも酸化力のつよいフッ素は、水と激しく反応し、酸素を発生する。 進研の問題は確かに基礎的な良問であるような気はしますが、だからと言って、あなたがそれで勉強できるかどうかは判りません。
394 .一酸化マンガンともいう.天然には緑マンガン鉱として産出する.炭酸マンガンを水素または窒素中で焼くか,をで還元すると得られる.灰緑色の粉末.塩化ナトリウム型構造.密度5. 名称 フッ化銀 塩化銀 臭化銀 ヨウ化銀 塩化鉛 II 臭化鉛 II ヨウ化鉛 II 組成式 AgF AgCl AgBr AgI PbCl 2 PbBr 2 PbI 2 色 黄色 白色 淡黄色 黄色 白色 白色 黄色 水への溶けやすさ 溶けやすい 溶けにくい 溶けにくい 溶けにくい 溶けにくい 溶けにくい 溶けにくい 熱水への溶けやすさ 溶けやすい 溶けにくい 溶けにくい 溶けにくい 溶ける 溶ける 溶ける 塩化水素(HCl) 塩化銀、臭化銀、ヨウ化銀には感光性があり、生じた沈澱に光を当てると銀が遊離する。 臭素やヨウ素も塩素と同様の反応で得られる。
3